الأسموزية ( تناضح ، حلول ) Osmosis
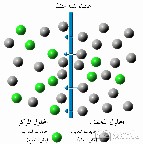
الاسموزية هي المرور أو الانتشار التلقائي للماء او أي سائل آخر من المحلول المخفف إلى المحلول المركز من خلال غشاء شبه منفذ ( غشاء يمنع مرور المواد المذابة ) ، و مثل هذه العملية هامة في الكيمياء و علم الأحياء ، و اول من لاحظ هذه الظاهرة الباحث أبي نوليت عام 1748 حيث لاحظ أنه عند فصل محلول للبول في الماء من الماء النقي بواسطة مثانة حيوان فإن الماء يمر خلال المثانة إلى محلول البول و لكن البول لا ينتقل إلى الماء . و من بعدها توالت الدراسات لفهم هذة الظاهرة حتى حلول العام 1854 حتى تم اطلاق اسم الأسموزية على هذه الظاهرة .
فإذا تم فصل المحلول عن المذيب النقي من خلال غشاء يسمح بمرور المذيب و لا يسمح بمرور المذاب فإن المحلول يصبح مخففا أكثر من خلال امتصاص المذيب خلال الغشاء و يمكن ايقاف تلك العملية من خلال زيادة الضغط على المحلول بكمية مناسبة يعرف باسم الضغط الأسموزي . و الضغط الأسموزي للمحلول المخفف من الخواص العامة للمحاليل بمعنى أن هذا الضغط يتناسب طرديا مع درجة تركيز المذاب في المحلول و لا يعتمد على طبيعة المادة المذابة ، و للمحلول المخفف فإن العلاقة بين الضغط الأسموزي π و حجم المحلولV و درجة الحرارة المطلقة Tتسمى معادلة فانت هوف و تكتب كما يلي :
πV = nRT
حيث R الثابت العام للغاز و يساوي 0.082 لتر ضغط جوي / مول.كلفن . و في حالة المحاليل تكون العلاقة ما بين الضغط الاسموزي و درجة التركيز بالمولارية كما يلي :
π = n/V RT= 0.082 MT
حيث π الضغط الأسموزي بوحدات جو ، و M المولارية للمحلول عند درجة الحرارة المطلقة T .



